Chloroquine
Chloroquine is een kinine en een van de geneesmiddelen tegen malaria. Daarnaast wordt het, omdat het ook het immuunsysteem licht onderdrukt, gebruikt bij de bestrijding van sommige auto-immuunziekten zoals reumatische artritis en lupus erythematodes. De stof is opgenomen in de lijst van essentiële geneesmiddelen van de WHO.
| Chloroquine | ||||
|---|---|---|---|---|
| Chemische structuur | ||||
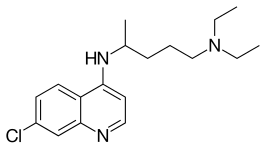
| ||||
| Farmaceutische gegevens | ||||
| Halveringstijd (t1/2) | 1-2 maanden | |||
| Gebruik | ||||
| Geneesmiddelengroep | Antiparasitaire middelen | |||
| Subklasse | Antimalariamiddelen | |||
| Merknamen | Nivaquine (Sanofi-Aventis) | |||
| Indicaties | Malaria profylaxe | |||
| Voorschrift/recept | Vereist | |||
| Toediening | Oraal | |||
| Dosering | 100 mg[1] | |||
| Databanken | ||||
| CAS-nummer | 54-05-7 | |||
| ATC-code | P01BA01 | |||
| PubChem | 2719 | |||
| DrugBank | APRD00468 | |||
| Chemische gegevens | ||||
| Molecuulformule | C18H26ClN3 | |||
| IUPAC-naam | N'-(7-chloroquinolin-4-yl)-N, N-di-ethyl-pentaan-1,4-diamine | |||
| Molmassa | 319,872 g/mol | |||
| ||||
Geschiedenis
bewerkenNa de Eerste Wereldoorlog zocht de Duitse regering naar alternatieven voor kinine als middel tegen malaria. Atabrine, een synthetisch analoog met hetzelfde werkingsmechanisme, werd in 1934 ontwikkeld door Bayer. Onderzoekers probeerden vervolgens structurele analogen te ontdekken met verbeterde eigenschappen. Twee daarvan waren chloroquine (1953) en hydroxychloroquine (1955). Nadat een studie in the Lancet in 1951 de effectiviteit van atabrine bij lupus had aangetoond, werden deze preparaten, voor chloroquine en hydroxychloroquine tot op heden, in de geneeskunde gebruikt ter bestrijding van inflammatoire polyarthritis en huidlupus.
Farmacologie
bewerkenChloroquine moet in vrij hoge dosis gegeven worden zodat de stof in alle organen van het lichaam wordt opgenomen. Chloroquine en andere kinines worden in verband gebracht met toxische effecten op het netvlies, zeker als gewerkt wordt met hogere doses gedurende een langere periode. De stof wordt in de lever gedeeltelijk omgezet in de actieve metaboliet desethylchloroquine.[2]
Malariapreventie
bewerkenChloroquine kan gebruikt worden ter preventie en bij bestrijding bij diverse soorten malaria: Plasmodium vivax, ovale en malariae. In zeer veel gebieden komen inmiddels stammen van chloroquine-resistente Plasmodium falciparum voor. Om die reden worden ook andere antimalaria-verbindingen gebruikt. Met name betreft het dan mefloquine of atovaquone. De combinatie van chloroquine met proguanil kan effectiever zijn bij de behandeling van chloroquine-resistente Plasmodium falciparum dan met chloroquine alleen. Tegenwoordig wordt deze combinatie niet meer door de (Amerikaanse) CDC aanbevolen, omdat er betere combinaties bekend zijn.[3]
Bijwerkingen
bewerkenBij de dosering die voor de bestrijding van malaria gebruikt wordt zijn de volgende bijwerkingen bekend: maagpijn, jeuk, hoofdpijn en accommodatieverlamming. Bij hogere doseringen worden deze problemen erger. Chloroquinetabletten hebben een onprettige metaalsmaak. Chloroquine mag slechts kortstondig toegediend worden. Bij inname over een langere termijn, maanden of zelfs jaren, kan chloroquine het gezichtsvermogen erg verminderen, met het risico op blindheid. Bij langdurig gebruik wordt daarom regelmatige controle door een oogarts aanbevolen.[4]
Werkingmechanisme
bewerkenDe malariaparasiet bevindt zich in het lichaam binnen in de rode bloedcel. Hier moet de parasiet het hemoglobine afbreken om de voor de parasiet essentiële aminozuren te verkrijgen voor de opbouw van zijn eigen eiwitten en zijn eigen metabolisme. Deze processen zijn noodzakelijk voor groei en deling van de parasiet. De vertering vindt plaats in het lysosoom (maagvacuole) van de parasitaire cel.
Tijdens dit proces komt de oplosbare en voor de parasiet giftige verbinding heem vrij. Dit molecule staat bekend onder de naam Fe(II)-protoporfyrine IX (FP). Om beschadiging door dit voor de parasiet gevaarlijke molecule te voorkomen wordt de heem door de parasiet gepolymeriseerd tot hemozoin,[5] een niet-toxisch molecule. Het hemozoin wordt in het lysosoom opgeslagen als onoplosbare kristallen.
Chloroquine komt de rode bloedcel en het lysosoom van de parasiet binnen door simpele diffusie. Chloroquine wordt in de zure maagvacuole (pH = 4,7) geprotoneerd tot CQ2+. In geladen vorm kan chloroquine de membranen niet meer door diffusie passeren. Door de CQ2+-moleculen worden de hemozoine-meloculen afgeschermd, waardoor verdere polymerisatie niet mogelijk is. Chloroquine bindt ook aan het heem (FP) zelf, waarbij een zeer giftig complex ontstaat (FP-chloroquine) dat de membraanfuncties van de cel verstoort. De gecombineerde actie van FP-chloroquine en FP resulteert in de lyse van de cel en uiteindelijk autodigestie. Uiteindelijk verdrinkt de parasietcel in zijn eigen metabolieten.
De effectiviteit van chloroquine ten opzichte van de parasiet is verminderd doordat sommige resistente vormen van de parasiet in staat zijn gebleken chloroquine uit het lysosoom te verwijderen. Resistente stammen doen dit ongeveer 40 keer efficiënter dan niet-resistente stammen. De genetische achtergrond is gerelateerd aan een aantal mutaties dat codeert voor trans-membraaneiwitten waaronder een zeer cruciale mutatie in het PfCRT-gen (Plasmodium falciparum Chloroquine Resistance Transporter). Dit gemuteerde proteïne is in staat chloroquine actief de cel uit te pompen. Resistente parasieten hebben vaak gemuteerde productie of vergrote expressie van ABC transporters, met name de PfMDR1 en PfMDR2 (Plasmodium falciparum Multi-Drug Resistance-genen). Deze zijn verantwoordelijk voor de chloroquinepompfunctie.
Het onderzoek naar het mechanisme van de werking van chloroquine en hoe de parasiet er resistent tegen is geworden is nog steeds gaande, en sommige zaken die in dit artikel beschreven zijn staan nog ter discussie. Andere theorieën met betrekking tot de werking van chloroquine gaan uit van een interactie met DNA of een combinatie van membraanfunctieverstoring en blokkade van de polymerisatie.
Bij bestrijding van reumatoïde artritis wordt gedacht aan de verhindering van lymfocytenverspreiding, het vóórkomen van phospholipase A, het verhinderen van vrijkomen van enzymen uit lysosomen, vrije zuurstofradicalen uit macrofagen, of de productie van IL-1.
Chloroquine (verkocht als Nivaquine) werd in België in 2016 uit de handel genomen zodat BCFI[6] of FAGG de bijsluiter niet meer vermelden.
Vermeende werkzaamheid tegen COVID-19
bewerkenTesten op SARS-coronavirus type 1
bewerkenDe werking van chloroquine tegen SARS-coronavirussen werd tijdens de SARS-epidemie in 2004 ontdekt door een team virologen van de KU Leuven, in het laboratorium van professor Marc Van Ranst.[7] Hier testte dit team in het biosafety level 3 (BSL-3) laboratorium van het Rega Instituut de activiteit van dit middel in celculturen, die besmet waren met het SARS-coronavirus type 1. Chloroquine bleek antiviraal te werken bij concentraties die bij de mens veilig kunnen gebruikt worden. Patiënten die gedurende een week chloroquine kregen, vertoonden minder koorts, hadden een sneller verbeterende longfunctie, en waren sneller weer virusvrij en genezen[8]. Echter, in augustus 2004 was de SARS-episode in China en Canada net voorbij, waardoor chloroquine toen niet verder bij patiënten kon worden getest.
Testen op SARS-coronavirus type 2 (SARS-CoV-2)
bewerkenOp 17 februari 2020 werd gerapporteerd door experten van het Chinese Ministerie van Wetenschappen en Technologie dat chloroquine bij klinische testen werkzaam bleek tegen het coronavirus dat COVID-19 veroorzaakt.[9] Het was getest in meer dan 10 ziekenhuizen in Beijing en de Chinese provincies Guangdong en Hunan. Bij de nieuwe studies rond het SARS-CoV-2 was het team virologen van de KU Leuven die de testen naar het SARS-coronavirus type 1 hebben uitgevoerd, niet meer betrokken. Er werden buiten de KU Leuven meerdere klinische studies met chloroquine uitgevoerd. Men ging na hoe effectief het middel is, hoeveel sneller patiënten genazen of hoe veel complicaties er werden voorkomen. Uit die studies blijkt dat chloroquine weinig of niet werkzaam is tegen infecties met SARS-CoV-2.[10][11] Tijdens een persconferentie van 20 februari 2020 van de wereldgezondheidsorganisatie werd aangegeven, dat er op dat moment geen bewijs is dat chloroquine een effectief middel is tegen COVID-19.[12] In Nederland kwam het RIVM in november 2020 tot het besluit dat gepubliceerde data van een groot aantal observationele onderzoeken en minimaal zeven RCT's met hydroxychloroquine vrijwel geheel consistent géén klinisch effect tonen ten opzichte van controles op het voorkomen van IC-opname of overlijden.[13] Van deze RCT's is ook een meta-analyse verschenen die geen effect op de 28 dagen mortaliteit en/of het risico op IC-opname laat zien.[14] De resultaten van de SOLIDARITY trial bevestigden deze conclusies opnieuw.[15] Artsen die in Nederland het middel voorschreven konden in 2021 daarvoor een boete krijgen van de Inspectie Gezondheidszorg en Jeugd.[16]