Baylis-Hillman-reactie
De Baylis-Hillman-reactie is een additiereactie uit de organische chemie, tussen een aldehyde en een ester, nitril, amide of keton van een α-β-onverzadigd carbonzuur, meestal acrylzuur (dus resp. een acrylaat, acrylnitril, acrylamide of vinylketon). De katalysator is een base, met name een nucleofiele amine zoals DABCO, pyrrocoline, chinuclidine of DBU.
Het algemeen schema van de reactie is:
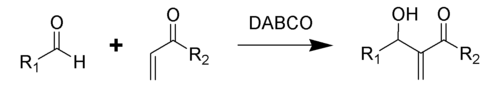
De reactieproducten zijn allylische alcoholen, die onder meer gebruikt worden als monomeer voor polymeren in kleefstoffen. Maar de reactie wordt ook op andere gebieden ingezet, bijvoorbeeld voor de synthese van natuurlijke stoffen of geneesmiddelen.[1]
De reactie is vernoemd naar de scheikundigen Melville E.D. Hillman en Anthony B. Baylis, die er in 1970 een octrooi voor aanvroegen ten behoeve van de Celanese Corporation.[2] Ze staat ook bekend als de Morita-Baylis-Hillman-reactie of MBH-reactie, waarbij Morita verwijst naar de Japanse scheikundige Ken-ichi Morita.
De reactie heeft een aantal voordelen: ze is atoomefficiënt; ze verloopt met vele verbindingen; en ze verloopt onder milde reactieomstandigheden, met een organische katalysator, dus zonder gebruik van zware metalen.
Reactiemechanisme
bewerkenDe alfa,bèta-onverzadigde carbonylverbinding of nitril (1, hier een keton) vormt met de amine die als katalysator fungeert (DABCO, 2) reversibel een nucleofiel intermediair zwitterion 3. Dat reageert met het elektrofiele aldehyde tot het keto-alcoholaat 4. Door transfer van een proton op de α-positie wordt de amine 2 weer afgesplitst en de dubbele binding in het allylisch alcohol 5 hersteld.[3]
Er blijkt ook een alternatief mechanisme te bestaan voor sommige aldehyden, waarbij in een tussenstap een tweede aldehydemolecule reageert tot de vorming van een intermediair hemiacetaal.[4][5]
- ↑ US. Patent Application 2007/0117822 A1, "Novel antimalarial Baylis-Hillman adducts and a process for the preparation thereof" van 24 mei 2007 aan Puli Narender et al.
- ↑ U.S. Patent 3743669, "Reaction of acrylic type compounds with aldehydes and certain ketones" van 3 juli 1973
- ↑ Portal für Organische Chemie: Baylis-Hillman-Reaktion
- ↑ Baylis–Hillman Mechanism: A New Interpretation in Aprotic Solvents Price, K. E.; Broadwater, S. J.; Jung, H. M.; McQuade, D. T.; Org. Lett., 2005, 7(1), 147-150. DOI:10.1021/ol047739o
- ↑ A New Interpretation of the Baylis–Hillman Mechanism Price, K. E.; Broadwater, S. J.; Walker, B. J.; McQuade, D. T. J. Org. Chem. 2005; 70(10); 3980-3987. DOI:10.1021/jo050202j