Natriumselenide
Natyriumselenide is een anorganische verbinding van natrium en seleen met de formule Na2Se. De verbinding wordt gesynthetiseerd in de reactie van seleen met natrium in ammoniak.[2][3]
| Natriumselenide | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
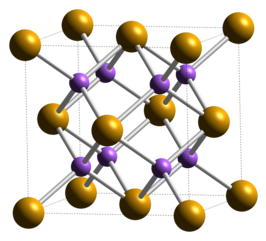
| ||||
| Algemeen | ||||
| Molecuulformule | Na2Se | |||
| IUPAC-naam | Natriumselenide | |||
| CAS-nummer | 1313-85-5 | |||
| Wikidata | Q418425 | |||
| Beschrijving | amorfe vaste stof | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Dichtheid | 2,62[1] g/cm³ | |||
| Smeltpunt | 875 °C | |||
| Oplosbaarheid in water | reageert g/L | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Net als de andere alkaliverbindingen van de chalcogeniden is ook natriumselenide zeer gevoelig voor vocht, waarbij een mengsel ontstaat van het diselenide en het hydroxide. De hydrolyse is het gevolg van de basesterkte van het Se2−-ion.
Ook oxidatie is een probleem bij deze verbinding waarbij polyselenides ontstaan. De stof verkleurt tijdens deze reactie van wit naar vuil-wit. Net als het vergelijkbare natriumsulfide dat tot waterstofsulfide reageert, vormt natriumselenide met zuren het giftige gas waterstofselenide gevormd.
Met elektrofielen worden seleenverbindingen gevormd:
Een vergelijkbare reactie treedt op met de andere laden van de koolstofgroep:
Veiligheid
bewerkenDe veiligheidsvoorschriften met betrekking tot natriumselenide beperken zich tot de opslag: bescherming tegen vocht en lucht (zuurstof).
- ↑ . Ed.: David R. Lide Handbook of Chemistry and Physics. (90th ed.) – CRC ISBN 9781420090840
- ↑ . (1963). Ed.: G. Brauer Handbook of Preparative Inorganic Chemistry 1. (2nd ed.) 421 – Academic Press (New York)
- ↑ 2nd Ed., 1963, NY. Vol. 1. p. 421.



